Un equipo del CSIC ha identificado el mecanismo que activa la respuesta inmune de la cavidad peritoneal frente a infecciones bacterianas. El estudio, publicado en la revista Immunity, describe cómo la formación de agregados de macrófagos peritoneales crea un microambiente crucial para el control de las infecciones.
Los macrófagos son células que pueden reconocer y eliminar células tumorales, microbios, restos celulares o sustancias extrañas.
La cavidad peritoneal –el espacio entre la pared y los órganos abdominales– está expuesta a graves patologías, como la sepsis y la metástasis de tumores derivados de cáncer de ovario, gástrico y colorrectal, por lo que es crucial conocer cómo el sistema inmune de esta zona responde de manera localizada ante dichas enfermedades abdominales.
“La sepsis se caracteriza por una respuesta desregulada del sistema inmune ante una infección, y es una de las principales causas de fallecimiento en todo el mundo”, explica Carlos Ardavín, investigador del CSIC en el Centro Nacional de Biotecnología (CNB-CSIC), quien ha liderado el grupo de investigación de este estudio. “Conocer los mecanismos de esta respuesta inmune es fundamental para poder combatir estas infecciones abdominales”, añade.
María López-Bravo, codirectora del trabajo junto a Ardavín en el CNB-CSIC, apunta: “Durante la sepsis peritoneal, los macrófagos eliminan las bacterias, y este proceso se asocia con la formación de agregados multicelulares en el mesotelio que cubre la cavidad peritoneal”.
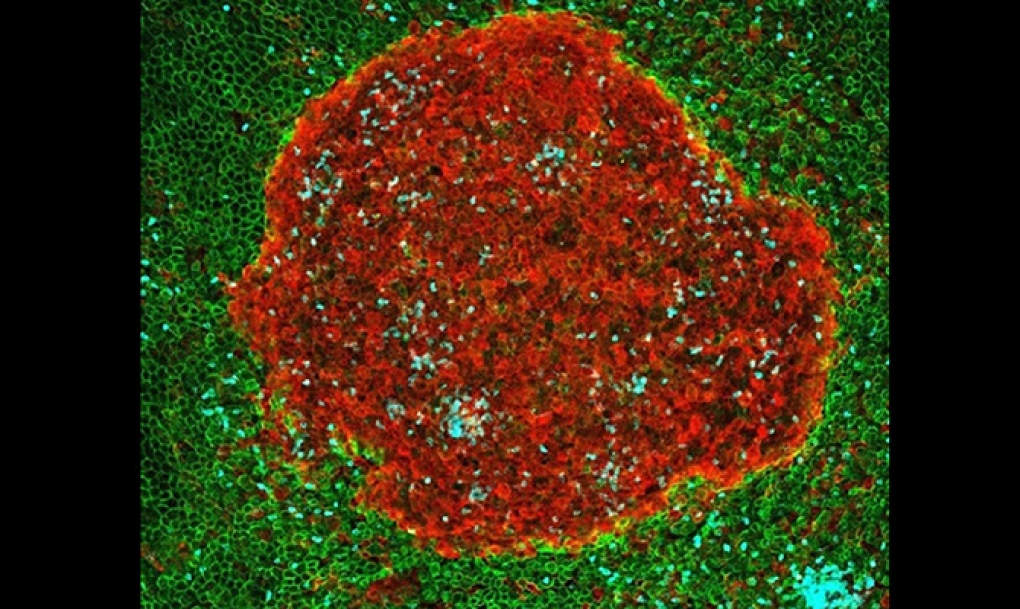
Mediante técnicas de microscopía confocal y citometría de flujo, en este trabajo “hemos caracterizado en detalle estas estructuras y las hemos denominado resMØ-aggregates (del inglés “resident macrophage aggregates”); estos agregados, que contienen también linfocitos B y neutrófilos, son estructuras dinámicas cruciales para controlar las infecciones en la cavidad peritoneal, ya que crean un microambiente en el que las células pueden realizar sus funciones antimicrobianas”.
Adrián Vega-Pérez y Laura Hernández Villarrubia, coautores del trabajo, explican cómo estas estructuras dependen de la formación de una red de fibrina (una proteína fibrosa que forma, junto con las plaquetas, los coágulos sanguíneos) por activación de un proceso de coagulación extravascular, controlado por las células mesoteliales que cubren la cavidad peritoneal. Una vez controlada la infección, los macrófagos peritoneales participan en la eliminación de células muertas presentes en el interior de los agregados, y contribuyen a la desintegración de estos por un proceso de fibrinólisis (degradación de la fibrina para deshacer los coágulos sanguíneos).
Ardavín destaca el cambio en la localización de los macrófagos, que en condiciones normales se encuentran libres en el fluido peritoneal, y pasan a formar los agregados, proporcionando así un soporte que facilita la interacción y la función de las células inmunitarias. Además, “la relevancia de la presencia de estas estructuras en la cavidad peritoneal abre un nuevo paradigma sobre la organización del sistema inmune de las diferentes cavidades corporales, y sugiere que podrían existir estructuras similares a las descritas en otras cavidades, como la cavidad pleural o los ventrículos cerebrales, con un papel crucial en la defensa frente a infecciones, un conocimiento clave para el desarrollo de nuevas terapias”.
Referencia científica:
Vega-Pérez A, Villarrubia LH, Godio C, Gutiérrez-González A, Feo-Lucas L, Ferriz M, Martínez-Puente N, Alcaín J, Mora A, Sabio G, López-Bravo M, Ardaví. ‘Resident macrophage-dependent immune cell scaffolds drive anti-bacterial defense in the peritoneal cavity’. Immunity. DOI: 10.1016/j.immuni.2021.10.007








Recordamos que SALUD A DIARIO es un medio de comunicación que difunde información de carácter general relacionada con distintos ámbitos sociosanitarios, por lo que NO RESPONDEMOS a consultas concretas sobre casos médicos o asistenciales particulares. Las noticias que publicamos no sustituyen a la información, el diagnóstico y/o tratamiento o a las recomendaciones QUE DEBE FACILITAR UN PROFESIONAL SANITARIO ante una situación asistencial determinada.
SALUD A DIARIO se reserva el derecho de no publicar o de suprimir todos aquellos comentarios contrarios a las leyes españolas o que resulten injuriantes, así como los que vulneren el respeto a la dignidad de la persona o sean discriminatorios. No se publicarán datos de contacto privados ni serán aprobados comentarios que contengan 'spam', mensajes publicitarios o enlaces incluidos por el autor con intención comercial.
En cualquier caso, SALUD A DIARIO no se hace responsable de las opiniones vertidas por los usuarios a través de los canales de participación establecidos, y se reserva el derecho de eliminar sin previo aviso cualquier contenido generado en los espacios de participación que considere fuera de tema o inapropiados para su publicación.
* Campos obligatorios