La Sociedad Española de Alergología e Inmunología Clínica (SEAIC) y la Sociedad Española de Inmunología Clínica, Alergología y Asma Pediátrica (SEICAP) han alertado sobre el riesgo vital que puede supener para los pacientes alérgicos graves no poder encontrar con normalidad autoinyectores de adrenalina en las farmacias debido a los problemas de suministro que se observan en España desde principios de 2018.
Como se recuerda desde estas organizaciones científicos, la adrenalina es el fármaco de elección para el tratamiento de la anafilaxia, la forma de presentación más grave de una reacción alérgica, por lo que los pacientes deben llevar siempre consigo esta medicación. La anafilaxia puede ser causada por una reacción alérgica grave a alimentos, medicamentos, picaduras de himenópteros (abejas o avispas), ejercicio, látex y otros alérgenos, y se caracteriza por afectar simultáneamente a varios órganos (piel, aparato respiratorio, digestivo, cardiovascular, etc.) y ser potencialmente mortal.
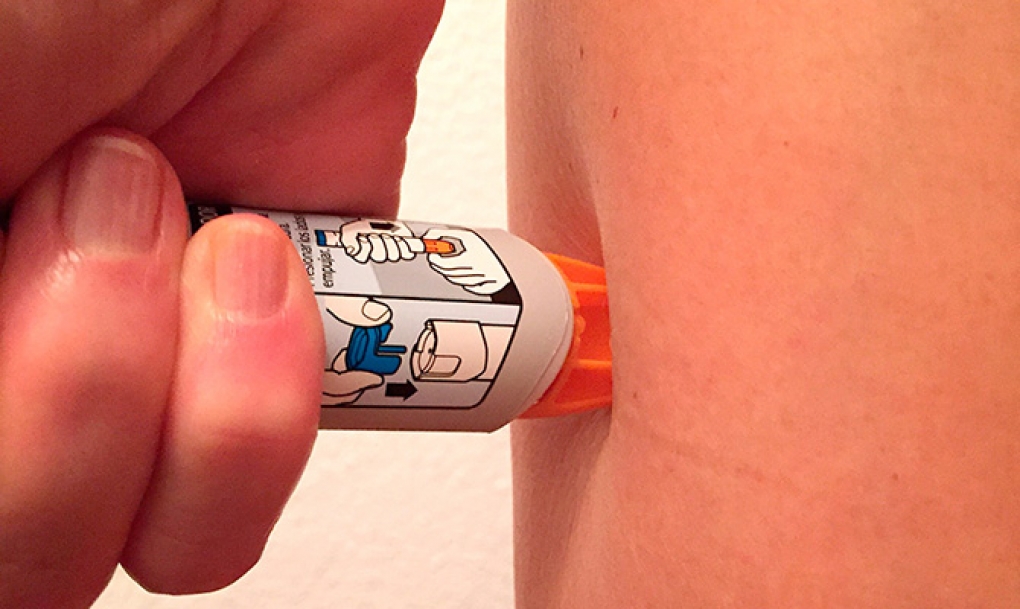
Ante una reacción anafiláctica, la adrenalina debe ser inyectada de forma intramuscular y precoz, ya que el retraso en su administración es un factor de riesgo para sufrir una anafilaxia muy grave o mortal. Por ello, a los pacientes que hayan sufrido una anafilaxia o presenten riesgo de sufrirla se les debe prescribir adrenalina, preferiblemente en dispositivos autoinyectores de adrenalina (AIA), que presentan la dosis exacta para administrarse en caso necesario, son de fácil manejo (incluso por niños) y evitan el riesgo de sobredosificación que conlleva la presentación en jeringa precargada de 1 mg.
Suspensión de la comercialización por la revisión de los precios
En enero de 2018, el laboratorio fabricante de la mayoría de los autoinyectores que se suministran en nuestro país emitió un comunicado sobre la suspensión temporal de comercialización de su producto. Dicha decisión estaba basada en los nuevos “precios de referencia” actualizados por el Ministerio de Sanidad, Consumo y Bienestar Social y la Agencia Española del Medicamento (AEMPS) para el año 2018 en la Orden SSI/1157/2017.
En este texto se agrupaba dentro del mismo conjunto de medicamentos todos aquellos productos con el mismo principio activo, sin tener en cuenta el dispositivo de administración. De este modo, se igualaba el precio de una solución inyectable que hay que cargar manualmente en una jeringa con el de una sofisticada pluma precargada que permite al paciente autoinyectarse con rapidez y seguridad ante una situación de emergencia. Para el laboratorio fabricante, la reducción del precio hacía insostenible el proceso de desarrollo y fabricación para España.
Mientras tanto, los otros tres fabricantes de autoinyectores no han podido asumir con su producción toda la demanda de producto, por lo que se están observando dificultades para encontrarlo.
Importados desde otros países
Según se explica desde la SEAIC y la SEICAP, la solución temporal por la que ha optado el Ministerio de Sanidad es importar el medicamento del extranjero (exportado a Europa desde la fábrica de Madrid por el mismo laboratorio que no lo comercializa en España). Esta situación es “incómoda para los pacientes”, continúan estas sociedades científicas, porque “les obliga a desplazarse a las delegaciones territoriales de Salud o a determinados hospitales para adquirirlo, y no siempre pueden disponer de un segundo autoinyector, como se recomienda”.
Además, aunque la falta de suministro no ha afectado a los dispositivos de uso pediátrico (con la mitad de producto en su interior), finalmente el problema también se ha extendido a estas presentaciones, ya que algunos pacientes y prescriptores están recurriendo a la doble administración del medicamento pediátrico, al no disponer de los autoinyectores propios de la edad adulta.
Tanto representantes de la SEAIC como de la SEICAP han mantenido reuniones con sociedades científicas, asociaciones de pacientes, técnicos, portavoces políticos de la Comisión de Sanidad en el Congreso, miembros de la Dirección General de Farmacia y representantes de los laboratorios farmacéuticos fabricantes con el objetivo de encontrar soluciones al problema actual en un breve plazo.
Según han manifestado responsables técnicos del Ministerio, la solución pasaría porque en el Parlamento Español se vote una modificación de la Orden SSI/1157/2017 que desvincule el dispositivo empleado en los AIA del precio de referencia de las ampollas de adrenalina. Sin embargo, “la inestabilidad política de los últimos tiempos ha impedido que se atienda convenientemente este problema en el Congreso de los Diputados, en detrimento de la seguridad y la calidad de vida de los pacientes con alergias graves”.
Por todo lo expuesto, “y temiendo que ocurra un acontecimiento grave relacionado con el desabastecimiento de un producto que salva vidas”, los representantes de ambas asociaciones científicas reclaman “una actitud activa por parte de los políticos y decisores para la puesta en marcha y aprobación de un Real Decreto que contemple excepciones a la Orden de Precios de Referencia o para la búsqueda de cualquier alternativa que permita que estos medicamentos lleguen a los pacientes”.








Recordamos que SALUD A DIARIO es un medio de comunicación que difunde información de carácter general relacionada con distintos ámbitos sociosanitarios, por lo que NO RESPONDEMOS a consultas concretas sobre casos médicos o asistenciales particulares. Las noticias que publicamos no sustituyen a la información, el diagnóstico y/o tratamiento o a las recomendaciones QUE DEBE FACILITAR UN PROFESIONAL SANITARIO ante una situación asistencial determinada.
SALUD A DIARIO se reserva el derecho de no publicar o de suprimir todos aquellos comentarios contrarios a las leyes españolas o que resulten injuriantes, así como los que vulneren el respeto a la dignidad de la persona o sean discriminatorios. No se publicarán datos de contacto privados ni serán aprobados comentarios que contengan 'spam', mensajes publicitarios o enlaces incluidos por el autor con intención comercial.
En cualquier caso, SALUD A DIARIO no se hace responsable de las opiniones vertidas por los usuarios a través de los canales de participación establecidos, y se reserva el derecho de eliminar sin previo aviso cualquier contenido generado en los espacios de participación que considere fuera de tema o inapropiados para su publicación.
* Campos obligatorios